当前位置:首页 > 锦秋A-Level频道 > A-level > 21年10月考试季考点解析 | A-Level化学U5考情回顾及备考指导
发布时间:2021-11-15 关键词: A-Level化学U5考情回顾
摘要:A-Level化学内容复杂考试难度又大如何才能拿到好成绩这着实是个问题,下面我们一起跟着锦秋回顾下爱德思考试局2021年10月考试季A-Level化学U5考情解析
21年10月考试季考点解析 | A-Level化学U5考情回顾及备考指导
A-Level化学内容复杂考试难度又大如何才能拿到好成绩这着实是个问题,下面我们一起跟着锦秋回顾下爱德思考试局2021年10月考试季A-Level化学U5考情解析!
A-Level化学U52021年10月考题分析
考试日期:2021年10月21日
考试时长:1小时45分
考试题目:共计21道
Q1、电极电势题。
(a) D 选择两个电极材料。左侧为气-液半电池,右侧为液-液半电池,两个半反应都不涉及固体反应物或产物,电极材料应皆为惰性金属。
(b) C 选择电解质成分。这个题HCl确实应该是最 佳选项,但H3PO4和H2SO4应该也是可选的,特别是课本上也写了可以用硫酸,此题有争议。
(c) B 计算电解质溶液成分。这个题非常新颖,在没有说明电解质溶液提及的情况下计算溶质质量。此题重点在于需根据重铬酸钾(K2Cr2O7)的质量计算其物质的量为0.05mol,而题干中说了是测定“标准电极电势”,也就意味着溶液中重铬酸根离子浓度是1mol dm-3,由此可以推算出溶液体积应为0.05dm3;或者干脆直接得出三价铬离子的量也是0.05mol。
(d) B 选择溶液2中的酸。注意此酸也是右侧半电池的反应物之一,选择此种酸的基本原则是避免带来更多的反应(与b问中原则基本一致),而硫酸和高铬酸有氧化性,氢溴酸有还原性。
Q2、C 电极电势题。写出电池图(电池符号),这种题目没有什么难度,电池图不过是反应方程式或者说半方程的一种书写形式而已,只是省略了箭头和电子,反应方向依然是自左向右;而此反应也不涉及固体物质参与,两个电极也都应该由铂构成。
Q3、A电极电势题。根据电池电动势推算反应自发,此题很常规。Ecell = Ered - Eox(还原电极的还原电势减去氧化电极的还原电势)= E1 + E2(按照半方程的反应方向改写后的两电极电势之和)。
Q4、D电极电势题。此题考查内容是比较全的。A项:电极电势的正负只是表示反应由左至右发生时的难易程度,跟正负极没有什么必然联系;B项:cathode是“还原电极”的意思,其词根”cata-”源于希腊语,意为“向下”,因为还原反应化合价下降,在原电池中对应中文的“正极”,在电解池中对应中文“阴极”;C项是对的:氧气确实在在负极(negative electrode/cathode)被还原;D项:在酸性和碱性条件下两个半电池的电极电势会有所不同,因为两种条件下半方程不同,但电池电动势(Ecell, cell potential)不受影响,因为总反应方程式不变。
Q5、B过渡金属题。找出一氧化碳毒性的最 佳解释。A项:一氧化碳与血红蛋白的结合并不是不可逆的,只不过平衡常数比较大,在实际的抢救过程中一氧化碳中毒的病人会使用高压氧舱(增大氧气分压)的方式救治就是因为此过程是可逆的;B项是对的;C项:气体与血红蛋白分子相结合的过程都是熵减的,毕竟都是由气态变为溶液状态;D项:一氧化碳中的三键并不是其毒性的原因,碳原子上的孤对电子才是。
Q6、D 过渡金属题。向钴离子溶液中加入氨和过量氨的变化,这种题目没有非常好的方法,只能是硬记。
Q7、B过渡金属题。配体交换反应中生成的(被换下来的)配离子越多则熵增越大,六齿配体EDTA无疑是最强的(一换六)。
Q8、D过渡金属题。(汽车尾气)催化转化器的原理,前三项都是对的,D项不对是因为生成的产物是氮气和二氧化碳,其中二氧化碳会引起温室效应,并不是完全无害。
Q9、D 过渡金属题。自催化反应即产物作催化剂的反应,三种产物中能作为催化剂的只有过渡金属二价锰离子。
Q10、A 过渡金属题。均相催化剂是通过分别与氧化剂和还原剂反应实现对反应的催化,无论是由氧化状态(Fe3+)还是还原状态(Fe2+)开始都可以。
Q11、D 芳香族题。氯代烃与苯在三氯化铝催化作用下发生傅-克反应,苯会依次替换三氯甲烷上的氯原子,但是不会替换氢原子。
Q12、C 芳香族题。苯酚与过量溴水反应最 大生成2,4,6-三溴苯酚(2,4,6-tribromophenol),分子式C6H3OBr3,摩尔质量330.7 g mol-1。
Q13、C 含氮有机物题。非常经典的胺的碱性题,由于脂肪烃基(直链)的推电子作用,氮原子上的孤对电子会更容易给出;而在芳胺中,苯环的离域π键会与氮原子的孤对电子共轭使其难以给出。
Q14、B 含氮化合物题。腈RCN的还原(亦可被称为加成)反应是将两条C-Nπ键进行加成,得到的产物中C和N上都会有两个氢,也就意味着只能得到伯胺(primary amine)。
Q15、B 含氮化合物题。判断多肽中的氨基酸是老生常谈的题目了,此处有四种R基(四种氨基酸):
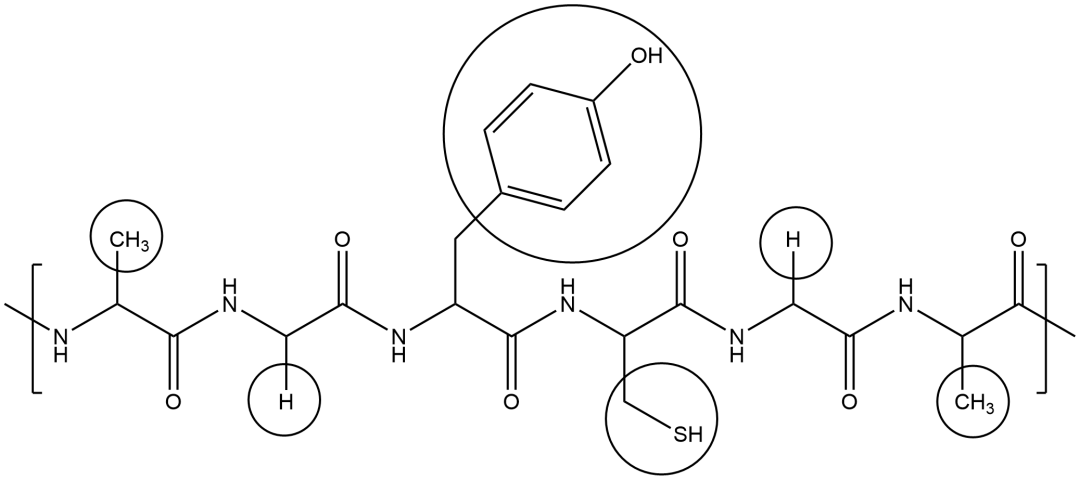
注意根据酰胺键/肽键来给多肽链断句。
Q16、D 有机合成(格氏试剂)题。这题比较有意思,需要亲手画一下才知道。A项:格氏试剂与水反应会生成醇,但只是将-MgBr换为-OH,并不必要是伯醇(primary alcohol);B项:醛与格式试剂反应也是生成醇,但如果是甲醛则会得到伯醇(primary alcohol)而非仲醇(secondary alcohol);C项:酮与格式试剂反应只能得到叔醇(tertiary alcohol)。如图:
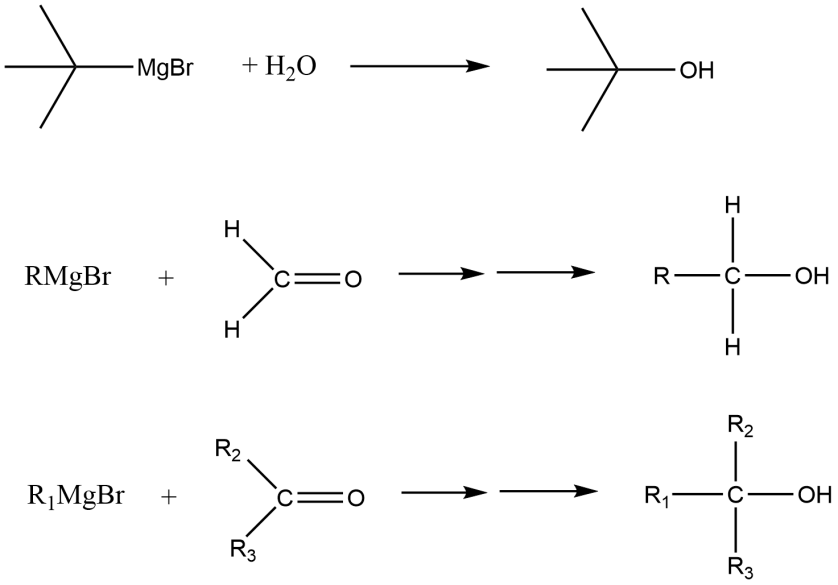
Q17、C 有机合成题。少量的杂质一定会降低物质的熔点并提升物质的沸点,在美系课本中还会额外的讨论杂质的量与熔沸点变化量的关系,在此处只需记住杂质会使熔点降低即可。
Q18、过渡金属题。题干有三个反应构成,第 一个反应是铁与盐酸反应生成浅绿色水合铁盐A,相对质量198.8;第二个反应是铁盐A溶于水生成含配离子B的浅绿色溶液,加入氰化钾生成配离子C,溶液变黄;第三个反应是C中通入氯气,生成配离子D,溶液变红,配离子D的钾盐E由其溶液结晶得到(此处注意断句)。
(a) 推导A的化学式。此题较为简单,仅需注意是铁单质与盐酸的反应即可。①iron react with HCl to produce FeCl2; ②
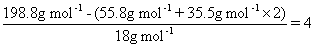 FeCl2·4H2O
FeCl2·4H2O
(b) 写出配离子B的化学式。实际是[Fe(H2O)6]2+,这个地方一般只要是水合亚铁离子即可,配位数无所谓。
(c) 已知配离子C有六个氰根离子配体,写出C的三维结构。需注意氰根离子是由碳上的孤对电子形成配位键,整个六氰合亚铁离子呈正八面体构型,另外整体带-4电荷。
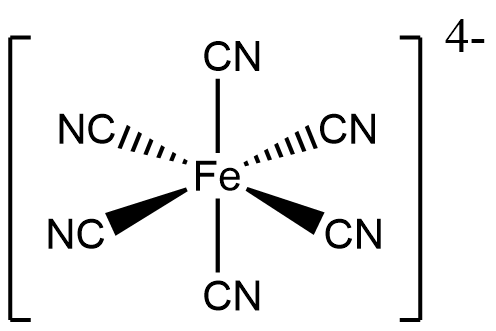
(d) 根据各元素质量分数推导E盐的经验式。传统的经验式题目。
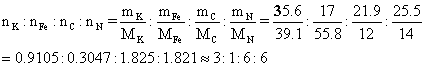
K3FeC6N6。
(e) 写出配离子C与氯气反应生成配离子D的离子方程。由(d)文可知E盐中的阴离子,也就是配离子D实际上就是六氰合铁(III)离子,于是方程式为:2[Fe(CN)6]4- + Cl2 → 2[Fe(CN)6]3- +2Cl-。
(f) 分辨题目中反应2和3的类型。反应2是六水合亚铁离子变成六氰合亚铁离子,当然是配体交换反应ligand exchange;反应3如(e)问所述,应该是氧化还原反应redox。
Q19、芳香族题。题干中叙述了最开始对苯结构的三种猜测,其中杜瓦式和拉登堡式后来被分离为单独的化合物了,但凯库勒式并不存在。
(a) 以化学反应区分杜瓦结构和苯。此题本身较为容易,即验证碳碳双键,选用溴水褪色bromine water decolourise或酸性高锰酸钾溶液褪色acidified KMnO4 decolourised。唯 一需要注意的是题目中说的“no compound with Kekule structure”,所以此处要区分的是杜瓦式与苯真正的离域电子式结构。
(b) 阐述在低分辨核磁共振氢谱中拉登堡结构和苯的相同点与不同点,需包含《数据册》中的数据。拉登堡式与苯的实际结构(离域电子式)的最 大相似之处就是都只有一种氢,即:only one peak on proton NMR。虽然拉登堡式中的峰会受到相邻氢的影响发生峰分裂,但对于低分辨核磁共振来说并看不出区别。不同之处当然是峰的化学位移(横坐标)不同:Ladenburg: -0.9~1.7ppm, benzene(delocalised π bond): 6.5~8.3ppm。
(c) 阐述X射线衍射中离域电子式和凯库勒式的区别。此处了解X射线衍射仪是用来看键长键角即可:all C-C bonds have same bond length in benzene; among Kekule structure, C=C would be shorter than C-C。
(d) 拉登堡式与杜瓦式皆异构化为苯(离域电子式),焓变分别为-376和-297kJ mol-1。(注意此处是isomerise [v. 异构化,变为同分异构体])
(i) 画出焓变图。
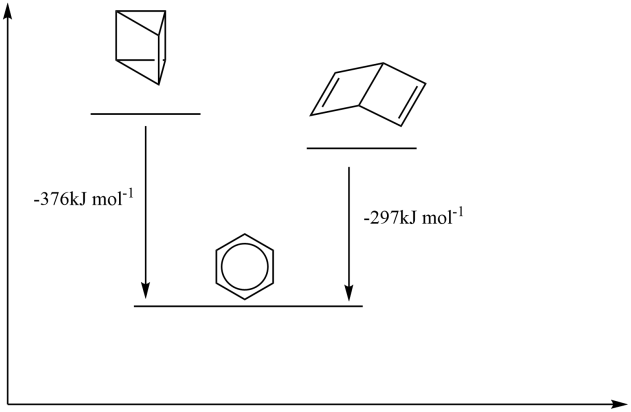
(ii) 阐述为何杜瓦式比拉登堡式活化能更低。此题只能从键角一个角度来解释,因为拉登堡式不仅包含共价键更多而且全是C-C单键,所以无法从成键数目得到有效结论:in Ladenburg structure, C-C-C bond angle is 60°and 90°(compare with 90°in Dewar structure),the 60°is further from (sp3 hybridisation) 109.5°bond angle。
(e) 已知己-3-烯氢化焓变为-118kJ mol-1;E-己-1,4-二烯为-236kJ mol-1; E-己-1,3-二烯为-214kJ mol-1,结合苯的知识,解释后二者与前者的联系。这个题就比较简单了,很明显 E-己-1,3-二烯有共轭(离域)π键:the E-hexa1,3-diene has delocalised(conjugated) π bond, makes it more stable than two isolated πbond; so E-hexa-1,3-diene is less exothermic than E-1,4-diene, which has exactly twice hydrogenation enthalpy than hen-3-ene (but still more exothermic than hex-3-ene which only addition with 1 mol of hydrogen molecules。
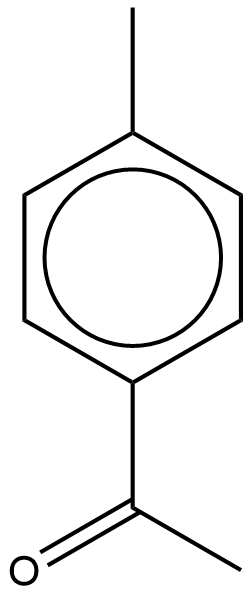
(f) 甲苯与乙酰氯在三氯化铝催化作用下生成CH3COC6H4CH3。
(i) 画出CH3COC6H4CH3的三种不同键线式。注意此处只能是乙酰甲苯,前述的结构式已经限制了其他的画法,也就是说画出的三个结构都必须是乙酰甲苯,并不仅仅是同分异构体。
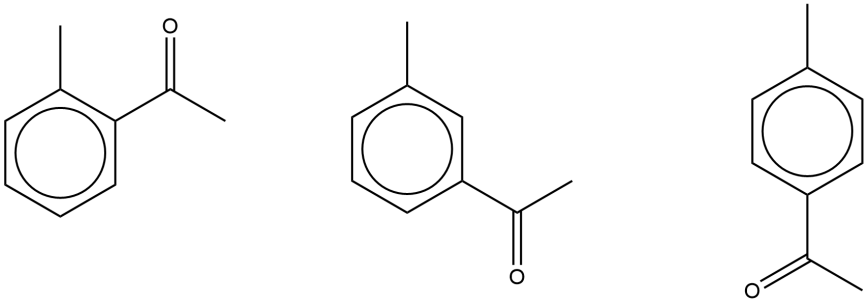
(ii) 其中一种结构X的核磁共振碳谱如图,以图中峰的个数辨认化合物X。此化合物中一共有9个碳原子,而图中仅有7个峰,说明有两对碳原子拥有完全相同的化学环境,那X只能是对乙酰基甲苯了:there are 9 carbon in compound but only 7 peaks on 13C-NMR spectrum, indicate that there are carbons with same chemical environments.
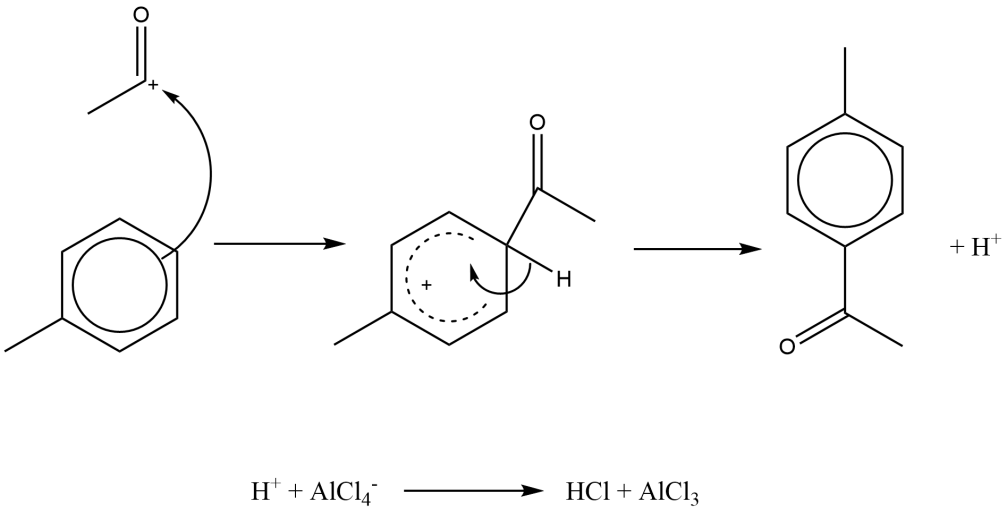
(iii) 完成反应机理,含催化剂重生方程式。注意生成的是对乙酰基甲苯。
Q20、过渡金属题。
(a) 氯化钛(III)被用作聚丙烯生产的催化剂。阐述如钛这样的过渡金属怎样的性质使得其化合物能够作有效的催化剂。这是一个异相催化剂原理题,固定答案:拥有3d轨道(亚层)可形成多于四条共价键transition metal has 3-d orbitals to form more than 4 covalent bonds.
(b) 氯化钛溶于四氢呋喃(THF)生成蓝色配合物Y。
(i) 四氢呋喃是单齿配体,解释“单齿”和“配体”。单齿即提供一对电子/形成一条配位共价键monodentate means provide one pair of electrons to form one dative covalent bond;配体是提供孤对电子与中心金属离子结合的物质ligand means the molecule provide one pair of electrons to form bond with centre metal cation。
化合物Z是Y的空间异构体,写出Z周围的配体排列。虽然是“空间异构”,但通过分析我们可以发现对于三(四氢呋喃)三氯合钛来说三个四氢呋喃配体只能由两种排列形式,其中Y的三配体共平面,如果不共平面的话也只有一种可能了:
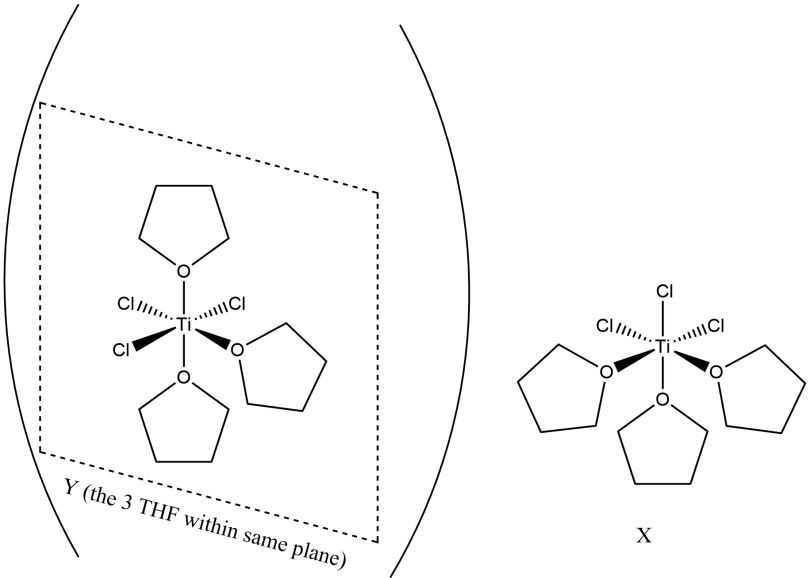
(c) 一学生想测定以氯化钛滴定硝酸镁时氮元素的氧化数(化合价)变化、
第 一步:以0.750g 六水合硝酸镁配置100cm3溶液。
第二步:量取10cm3溶液,加入茜素(alizarin)指示剂。加入2cm3浓盐酸并加热混合物。
第三步:将0.0850mol dm-3的氯化钛溶液装入滴定管中,一边加热一边滴定第二步中的混合物。
滴定过程中Ti3+离子被氧化为TiO2+,茜素指示剂在Ti3+中呈绿色而TiO2+中呈黄色。滴定值为20.70cm3。
(i) 陈述滴定终点时溶液颜色变化。Green to yellow。
(ii) 以结果推断氮元素的最终氧化态。
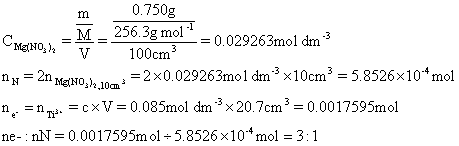
Final state is N2+ or NO。
(iii) 利用电极电势和(ii)中的答案写出滴定反应中的总离子方程式。硝酸根离子被还原的倾向很强,三个还原反应都能发生,通过前一问可知最终反应产物为一氧化氮。
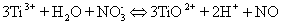
(iv) 计算电池电动势。Ecellθ= +0.96V - (+0.10V) =+0.86V。
(v) 解释加热锥形瓶内容物的原因。此反应常温下即自发,加热无非就是提高反应速率: increase reaction rate。
(vi) 老师说:因为TiCl3蓝色而TiO2+无色,反应可不加茜素指示剂。评价老师的说法,需包含:辨认TiCl3水溶液中的有色离子;解释颜色如何产生;提议为何加茜素指示剂结果更准确。典型的小拼大型六分大题。得分点包括:
① hexahydrated titanium(III) ion, [Ti(H2O)6]3+; ② (the water ligands donate electron pairs to centre atom,) 3-d orbitals of Ti energy level split; ③ electrons absorb energy (from light) to promote/excited to higher energy level; ④ to reflect/transmit coloured light; ⑤ yellow colour of [Ti(H2O)6]3+ (may be) pale; ⑥ alizarin indicator makes end point more visible。
Q21、有机综合题。
完成姜黄素(curcumin)与自由基T·反应的方程式。类比于自由基取代反应的增殖步(propagation step)即可。

(b) 连接在蛋白质侧链上的硒(Se)离子会与姜黄素进行亲核加成反应,完成下述机理。
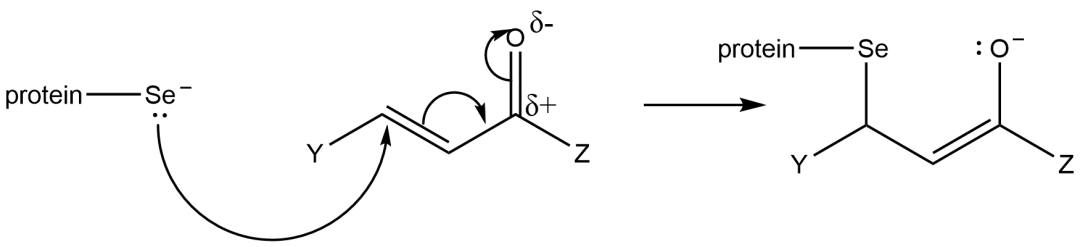
(c) 姜黄素阴离子可作二齿配体,形成金属-姜黄素配合物(M-curc),两个氧原子会配位在相邻的位置。完成下表。

表中比较难填的就是形状了,对于四配位的化合物来说会有正四面体与平面四方两种可能,二姜黄素合金离子中键角是90°,就排除了正四面体的可能。
(d) 由2-硝基苯甲醛和苯胺合成甲基红的步骤如下。
(i) 陈述X步中的试剂与反应条件。X步是将苯甲醛氧化为苯甲酸,酸性重铬酸钾与酸性高锰酸钾皆可:H2SO4 + K2Cr2O7, reflux。
画出化合物A的结构。2-硝基苯甲酸与还原剂锡金属、盐酸反应会被还原为芳胺:
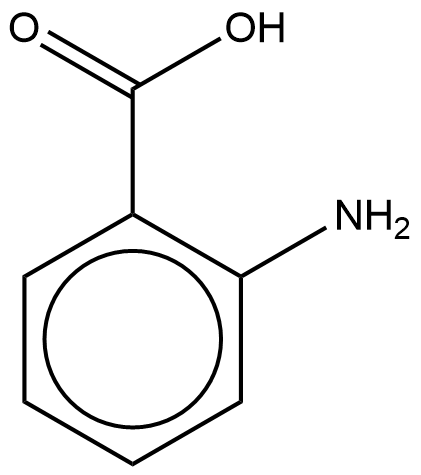
(iii) 写出Y步骤的试剂。Y是芳胺生成偶氮苯的反应,试剂为NaNO2 (HNO2) + HCl
(iv) 写出化合物B的结构。由B的反应物苯胺和B与偶氮苯反应得到的产物可知,苯胺与碘代甲烷发生了亲电取代反应,生成了N,N-dimethylphenylamine,即:
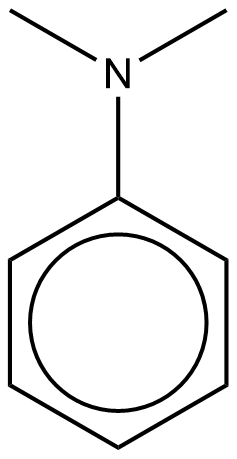
(v) Y和Z反应须将温度控制在接近5℃,陈述温度过高或过低的影响。温度较高是经常问的,会使得偶氮苯分解/与水反应,生成苯酚:when temperature higher than 5℃ the benzene diazonium chloride will decompose to produce phenol;温度过低之前没有问过,但也能很快想出来反应会过慢the reaction will be too slow。
(e) (染料)靛蓝可由2-硝基苯甲醛与丙酮在氢氧化钠水溶液中反应得到。
(i) 完成反应方程式。此处没有太好的方式,只能是写出分子式然后配平,反应的分子方成为:2C7H5NO3 + 2C3H6O + 2NaOH → C16H10N2O2 + 2C2H3O2Na + 4H2O。
(ii) 计算在85%产率的情况下,制备10.0g靛蓝所需的苯甲醛质量。
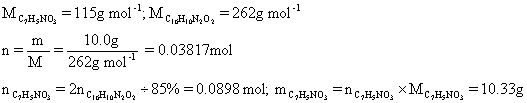
(f) 写出香豆素(coumarin) 440与以下物质反应的有机产物结构。
(i) 与过量氢氧化钠发生水解。会造成香豆素中的酯键断裂。
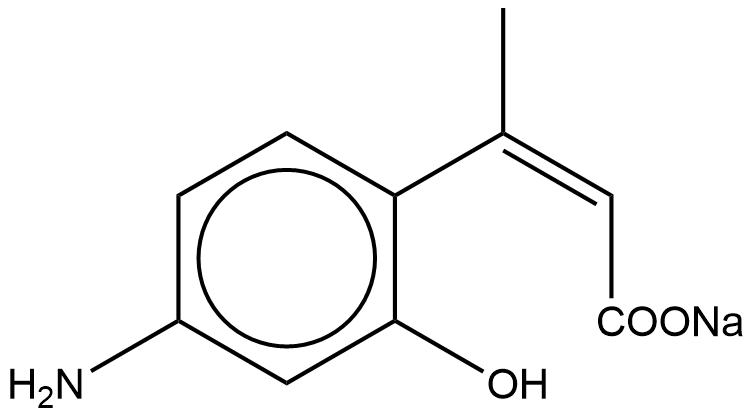
(ii) 与乙酰基氯缩合。乙酰基氯会与胺基缩合。